L’imagerie en totale mutation
S’il est un domaine médical dans lequel le Big Data s’est imposé d’emblée, c’est celui de l’imagerie médicale. Robots IRM, Pet Scans, les praticiens disposent de moyens d’imagerie de plus en plus sophistiqués et l’arrivée de la 3D n’a fait qu’ajouter à l’accroissement des volumétries à traiter. Pour y faire face, les professionnels s’organisent, à l’image du projet Région sans Film, une plateforme cloud d’Imagerie médicale partagée (IMP) à disposition des établissements de santé et des médecins de ville. Son objectif : mutualiser les coûts liés au stockage et l’archivage sur le long terme. Son ambition : stocker jusqu’à 700 Pétaoctets dans des fichiers devant être conservés 15 ans !
Outre le volet partage et stockage de données graphiques, de multiples travaux sont menés depuis les années 80 dans ce que l’on appelle désormais CAD (Computer Aided Diagnosis). L’idée est ici que la machine peut utilement seconder le praticien, en précision et en vitesse, dans la détection de nodules potentiellement cancéreux sur une radio ou de zones de métastases sur une scintillographie. A côté des algorithmes d’amélioration d’image et de reconnaissance de forme que l’on pourrait rapprocher de ceux utilisés pour l’analyse de clichés satellites, les chercheurs développent des fonctions très spécifiques. Exemple type : l’identification de pathologies cardiaques à partir d’une succession d’images IRM permettant de recréer la cinématique d’un cœur en train de battre.
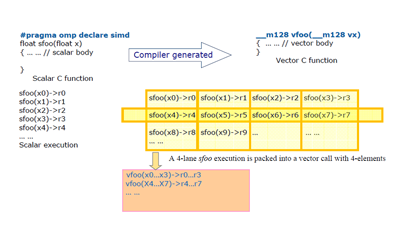
L’analyse des images tire très directement profit des techniques de programmation des FPGA et GPU mises au point sur les grands calculateurs académiques. Spécialisé dans les systèmes de dépistage des cancers du sein, l’américain Hologic, par exemple, exploite CUDA pour permettre aux radiologues d’obtenir en temps réel des clichés issus d’appareils d’imagerie médicale. Par rapport à un traitement CPU classique, le speedup atteint 250X. De plus, l’utilisation de GPU permet la miniaturisation des plateformes, ce qui les rend à la fois portables et compatibles avec une utilisation en salle d’opération.
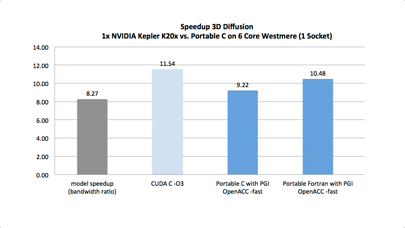
Les travaux de David Fuentes, du Centre de traitement du cancer MD Anderson de l’université du Texas, illustrent parfaitement cette tendance. En 2012, le Dr Fuentes a développé un code permettant de calculer l’échauffement des tissus cérébraux lors d’un traitement laser. Comme de multiples paramètres entrent en ligne de compte dans ce calcul (propriétés des matériaux, conductivité thermique, propriétés optiques, circulation sanguine…), ce code était suffisamment complexe pour mobiliser le calculateur Ranger du TACC. Un an après, des chercheurs de Rice sont parvenus à le porter en OpenCL pour le rendre exécutable sur un simple accélérateur GPU du marché. Là où l’obtention de résultats nécessitait une douzaine d’heures de calcul sur environ 12 cœurs CPU, 10 à 12 secondes y suffisent désormais.
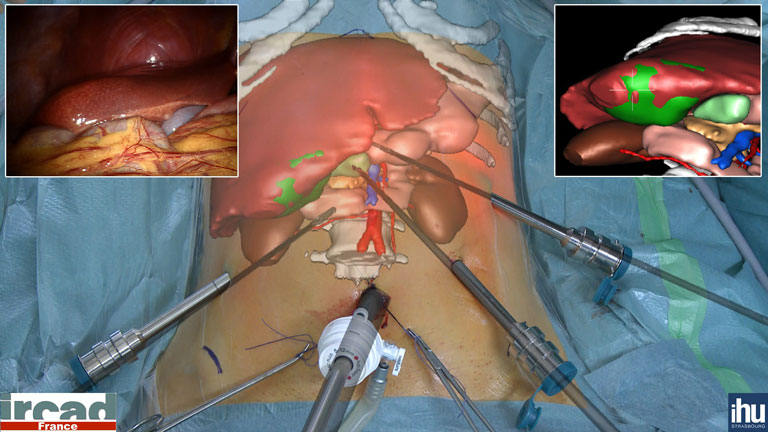
Basée sur la simulation, la réalité virtuelle permet aux chirurgiens de se former et de répéter des gestes délicats avant une opération complexe.
Autre domaine extrêmement prometteur en termes de résultats cliniques, la modélisation 3D à partir d’images 2D. De nombreux laboratoires dans le monde travaillent sur le sujet, et notamment l’IRCAD (Institut de recherche contre les cancers de l’appareil digestif) du CHU de Strasbourg, créé par le professeur Jacques Marescaux. Avec ses antennes à Taïwan et au Brésil, l’institut forme chaque année 3 500 praticiens à la chirurgie mini-invasive. Son centre d’excellence, animé par une équipe de R&D de pointe, travaille sur des techniques de réalité virtuelle et de réalité augmentée pour former les médecins et les assister lors des opérations. Parmi ses réalisations les plus emblématiques, il faut citer Visible Patient, un ensemble de logiciels et de modélisations du corps humain incluant une bibliothèque librement accessible de 2 000 modèles 3D correspondant à des cas cliniques anonymes. Médecins et chirurgiens peuvent y télécharger des modèles, les consulter avec l’application de visualisation développée en interne et étudier en trois dimensions les pathologies auxquels ils vont avoir affaire. Ils peuvent également y transférer au format standard DICOM (Digital Imaging and Communications in Medicine) les images IRM ou de tomographie numérique de leurs patients, et les comparer aux modèles 3D correspondants. En pratique, le praticien dispose des outils pour simuler l’opération dans une situation aussi proche que possible de la réalité et la répéter autant de fois que nécessaire, jusqu’à maîtriser parfaitement le geste à accomplir.
More around this topic...
© HPC Today 2024 - All rights reserved.
Thank you for reading HPC Today.